Предлежание и аномальное прикрепление плаценты: современные подходы к диагностике и ведению беременности
 Статья из журнала “Медицинские аспекты здоровья женщины” № 1 (1)за май 2006 года
Статья из журнала “Медицинские аспекты здоровья женщины” № 1 (1)за май 2006 года
Изучение плаценты имеет многовековую историю, за это время пройден путь от макроскопического описания до современных молекулярно-биохимических исследований. Однако, несмотря на достижения в ранней диагностике и лечении нарушений взаимосвязи функциональной системы мать-плацента-плод, в практическом акушерстве остаются проблемы, связанные с развитием плаценты, актуальность которых не утрачивается из-за большого количества осложнений беременности и родов. Частота встречаемости предлежания плаценты составляет 0,2-0,9%, однако продолжает оставаться одним из наиболее серьезных факторов развития акушерских кровотечений и перинатальных потерь. Ситуация усугубляется тем, что предлежание сочетается с разнообразными вариациями аномального (глубокого) прикрепления плаценты к стенке матки (plаcenta adhaerens, accreta, increta, percreta). В этом случае особое значение приобретает своевременная диагностика данной патологии, позволяющая оптимально подготовиться к родоразрешению. Целью нашей работы было изучение сочетания предлежания и аномального прикрепления плаценты у женщин с отягощенным анамнезом. На примере двух клинических случаев проанализированы возможности современных методов диагностики и ведения беременности и родов.
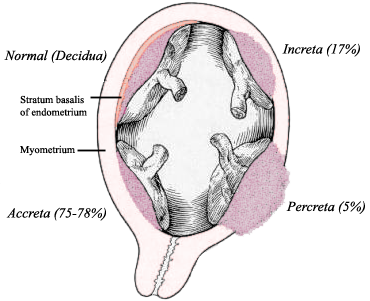 На картинке наглядно показаны нормальная плацентция и три вида патлогического прикрепления плаценты, а также частота вожникновения данного осложнения.
На картинке наглядно показаны нормальная плацентция и три вида патлогического прикрепления плаценты, а также частота вожникновения данного осложнения.
Материал и методы исследования
Ультразвуковое исследование (УЗИ) пациенткам в динамике беременности проводилось с помощью аппарата «Антарес» фирмы «Сименс» (Германия) с использованием цветного допплеровского картирования. Кесарево сечение в обоих случаях выполнялось под эпидуральной анестезией с применением аутодонорства.
Описание случаев
Случай 1. Пациентка К., 35 лет, после экстракорпорального оплодотворения (ЭКО) обратилась в отделение амбулаторной помощи для УЗИ в 32 недели беременности. При УЗИ установлено центральное предлежание плаценты. На основании использования цветного допплеровского картирования заподозрено плотное прикрепление плаценты (plасеnta adhaerens). В дальнейшем беременность протекала без особенностей. Пациентка поступила на профкойку в акушерское отделение клиники с диагнозом: беременность II, 35 недель; центральное предлежание плаценты, подозрение на аномальное прикрепление; неустойчивое положение плода ЭКО; отягощенный акушерско-гинекологический анамнез (бесплодие, клиновидная резекция яичников); ожирение I степени; миокардиодистрофия, сердечная недостаточность (СН) 0.
У беременной установлена группа крови B (III) Rh-отрицательная принадлежность, что осложняло ситуацию с учетом предстоящих родов и возможного кровотечения. При сроке беременности 38-39 недель в плановом порядке проведено родоразрешение путем корпорального кесарева сечения. Извлечена живая доношенная девочка массой тела 3480 г, ростом 51 см, с оценкой по шкале Апгар 8-8 баллов. При осмотре матки и придатков обнаружено центральное предлежание плаценты, придатки матки – без особенностей. Плацента осторожно отделена и выделена с некоторыми затруднениями ввиду наличия интимного прикрепления (placenta adhaerens). Полость матки протерта марлевой салфеткой, при осмотре выявлено наличие кровоточащих участков в области нижнего сегмента и шейки матки. С целью сохранения матки решено попытаться выполнить гемостаз. Кровоточащие участки прошиты и лигированы викрилом. Кровотечение уменьшилось, однако полный гемостаз не достигнут. Решено произвести перевязку маточных сосудов. Маточные сосуды прошиты и лигированы на уровне внутреннего зева шейки матки. Кровотечение прекратилось. Далее целостность матки восстановлена двухрядным (викриловым) швом. После того, как хирурги убедились в наличии гемостаза, брюшная стенка ушита, оставлен дренаж в брюшной полости. Общая кровопотеря составила 800 мл. Послеоперационный период протекал гладко. Пациентка выписана домой на 8-е сутки в удовлетворительном состоянии.
Случай 2. Пациентка Б., 32 года, наблюдалась в отделении амбулаторной помощи с 8-й недели беременности. В анамнезе – четверо родов путем операции кесарева сечения. Трое детей погибали на 2-е сутки после рождения, причина смерти неустановлена. Для исключения хромосомной патологии у плода (в связи с отягощенным анамнезом) в сроке 16 недель произведены трансабдоминальный амниоцентез, биопсия плаценты. Кариотип плода – 46, ХY. Трижды во время беременности пациентка лечилась по поводу антифосфолипидного синдрома. При УЗИ на 26-й неделе выявлено многоводие. Плацента располагалась по передней стенке матки, в области нижнего сегмента и рубца, частично перекрывая внутренний зев. В 32 недели при УЗИ с допплерографией обнаружены центральное предлежание плаценты, признаки плацентарной недостаточности. Передняя стенка матки была значительно деформирована, мышечный слой в некоторых местах четко не визуализировался, что позволило предположить аномальное прикрепление плаценты. Женщина после лечения в отделении патологии беременных переведена в акушерское отделение для планового кесарева сечения с диагнозом: беременность 37-38 недель; поперечное положение плода; центральное предлежание плаценты; плацентарная недостаточность; четыре рубца на матке.
При вскрытии брюшной полости, на фоне выраженного спаечного процесса, обнаружено отсутствие мышечного слоя значительной части передней стенки матки, предлежание в рану плаценты и плодного пузыря, спаянных с апоневрозом. Через плаценту за ножки извлечен живой доношенный мальчик с оценкой по Апгар 8-8 баллов, весом 3100 г, ростом 50 см. Плацента осторожно отделена, при отделении обнаружено ее плотное прикрепление в области внутреннего зева. Определена повышенная кровоточивость плацентарной площадки в месте плотного прикрепления. Учитывая желание женщины сохранить матку, произведена перевязка внутренних подвздошных артерий. Однако кровотечение не прекратилось, и была произведена экстирпация матки.
Хотелось бы отметить анестезиологическое обеспечение и особенности предоперационной подготовки. В обоих случаях решено провести аутодонорство и восполнить интраоперационную кровопотерю аутологичной кровью. Одной из причин для принятия такого решения была невозможность подготовки нескольких доз свежезамороженной нативной плазмы из-за трудностей, связанных с введением карантина. Кроме того, редкая группа крови беременной женщины в первом случае не позволяла иметь в запасе большое количество эритроцитарной массы. Пациенткам объяснены преимущества данного метода, получено их письменное согласие.
За два сеанса заготовлено 600 мл цельной крови для первой пациентки (в первый сеанс – забор 300 мл крови и восполнение 1000 мл 0,9% раствора хлористого натрия (NaCl); исходный гемоглобин – 110 г/л, после первого сеанса – 108 г/л. Во время второго сеанса, через двое суток, заготовлено 600 мл, восполнено – 300 мл аутологичной крови и 1000 мл 0,9% раствора NaCl; гемоглобин снизился до 102 г/л). Забор производился под тщательным мониторным наблюдением (артериальное давление, пульс, электорокардиография, пульсоксиметрия), последний сеанс был проведен за двое суток до операции.
По желанию беременных в обоих случаях операция начата под эпидуральной анестезией (перед операцией было оговорено, что при расширении объема оперативного вмешательства или начавшемся кровотечении будет произведена интубация трахеи и проведен эндотрахеальный наркоз с тотальной в/в анестезией).
После извлечения ребенка первая пациентка находилась в сознании, ребенок сразу приложен к груди и через 20 минут транспортирован в отделение неонатологии. После этого пациентке начато в/в введение гипнотика (диприван 50 мг/кг/час). Стабильность гемодинамики, отсутствие гипоксии и респираторных расстройств, адекватная скорость восполнения кровопотери определили продолжение анестезии на спонтанном дыхании. В начале ушивания брюшной полости в/в введение гипнотика прекращено, к окончанию операции сознание женщины восстановлено полностью. За период оперативного вмешательства (включая инфузию перед выполнением эпидуральной анестезии) в/в введено: кристаллоидов 1500 мл, гидроксилэтилкрахмала 500 мл, аутологичной крови (после остановки кровотечения) – 600 мл). В послеоперационном периоде гемоглобин умеренно снижался до 94 г/л, послеоперационный период протекал без особенностей и осложнений. При переводе на 2-е сутки из палаты интенсивной терапии в послеродовое отделение пациентка оценила свое состояние во время операции как комфортное, а обезболивание путем пролонгированной эпидуральной анестезии в послеоперационном периоде – адекватным.
Во втором случае забор аутологичной крови был затруднен временем, отведенным на подготовку к оперативному вмешательству. По настоятельной просьбе пациентки операция перенесена на сутки раньше назначенного срока, что не позволяло полноценно за два сеанса провести забор крови. Принято решение провести за трое суток до операции сеанс аутодонорства в несколько большем объеме. Произведен забор 420 мл аутокрови с восполнением 500 мл рефортана и 1000 мл 0,9% раствора NaCl. Уровень гемоглобина – 98 г/л.
Операция начата под эпидуральной анестезией, после извлечения ребенок приложен к груди. Через 15 минут, в связи с начавшимся кровотечением, пациентка переведена на искусственную вентиляцию легких (ИВЛ), в дальнейшем операция проводилась под эндотрахеальным наркозом. Кровопотеря во время операции составила 1300 мл, восполнение: 500 мл рефортана, 500 мл гелофузина, 2500 мл 0,9% раствора NaCl, 230 мл антигемофильной плазмы, 420 мл аутологичной крови. В раннем послеоперационном периоде в течение трех часов продолжалась ИВЛ в условиях операционной. Учитывая отсутствие признаков продолжающегося кровотечения, стабилизацию показателей коагулограммы, уровень гемоглобина (82 г/л), стабильную гемодинамику, пациентка переведена на спонтанное дыхание и транспортирована в палату интенсивной терапии. Послеоперационный период протекал без особенностей на фоне анемии I-II cтепени.
Обсуждение результатов
Предлежание плаценты наиболее часто возникает у повторнобеременных и повторнородящих. Раньше основными факторами для возникновения этой патологии считались воспалительные процессы после абортов, родов. Современные исследования свидетельствуют о том, что первопричиной предлежания и аномального прикрепления плаценты являются бластопатии, возникающие на фоне особенностей строения маточной стенки (в основном дистрофических изменений) после перенесенных внутриматочных вмешательств, операций, особенно кесарева сечения.
Патология бластогенеза, кроме нарушения гаметогенеза, включает в себя все патологические процессы в бластоцисте, в том числе возникающие при ее имплантации в эндометрий в течение первых 12-15 суток после оплодотворения. Хотя бластопатии относятся сегодня к наименее изученным разделам антенатальной патологии, известно, что некоторые патологические процессы, происходящие в них, имеют отстроченное действие, которое не представляет серьезной угрозы для развития эмбриона и плода, однако грозит осложнениями в раннем послеродовом периоде. Речь идет о нарушении глубины имплантации бластоцисты.
Глубокая имплантация бластоцисты приводит, прежде всего, к формированию аномальных форм плаценты, таких как двудолевая, окончатая, поясная, окруженная ободком, валиком (рис. 1).
Более серьезной формой глубокой имплантации является аномальное прикрепление плаценты. Вследствие особенностей строения мышечной и слизистой оболочек нижнего сегмента матки ворсины плаценты проникают глубже, чем при ее локализации в теле матки. В связи с этим часто возникает плотное прикрепление (placenta adhaerens), иногда истинное приращение плаценты. В результате нижний сегмент матки превращается в своеобразную кавернозную ткань, которая плохо сокращается и легко травмируется; процесс отслойки плаценты в родах нарушается, что приводит к маточному кровотечению и возникновению геморрагического шока.
Процессы формирования и имплантации плаценты находятся в прямой зависимости от уровня метаболизма в эндометрии и активности ряда ферментов.
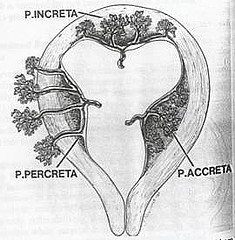
Pl. accreta/increta/percreta различаются между собой только степенью внедрения ворсин плаценты в миометрий. Эта классификация – условна, практически все три степени внедрения могут быть представлены у одной беременной, поэтому чаще употребляется термин increta (рис. 2).
Лучшим методом диагностики аномалий предлежания и прикрепления плаценты считается УЗИ, которое помогает не только своевременно выявить данную патологию, но и предположить ее развитие в ранние сроки беременности.
В конце первого триместра беременности плацента в 25-42% случаев полностью или частично перекрывает внутренний зев. В динамике беременности частота предлежания плаценты значительно уменьшается со сроком гестации. Это связано с миграцией плаценты, вызванной тем фактом, что свободная стенка матки растет быстрее, чем занятые плацентой участки [3].
В современных исследованиях установлено, что миграция плаценты частично зависит от трофотропизма, при котором плацентарная ткань атрофируется на менее оптимальной стороне имплантации и гипертрофируется на более оптимальной. К примеру, в 20 недель беременности плацента покрывает 1/4 поверхности миометрия, в конце беременности – 1/8.
По данным R.H. Becker et al. (2001), у обследованных с помощью эхографии более 8 тыс. беременных выявлено, что частота низко расположенной и предлежащей плаценты снизилась с 1,78% в 20 недель до 0,8% в 23 недели гестации [2].
Многие авторы предпринимали попытки прогнозирования предлежания плаценты в родах на основании данных УЗИ. Полученные результаты позволили сделать вывод о том, что, если в 23-25 недель гестации плацента перекрывает внутренний зев на 25 мм и более, возможность ее предлежания (полного или частичного) перед родами приближается к 60% [5].
Что говорит по этому поводу доказательная медицина? В методах, эффективность которых доказана, но не подтверждена в рандомизированных исследованиях, есть только один пункт, регламентирующий важность эхографии: повторное УЗИ на 32-й неделе беременности при низком расположении плаценты. Очевидно, до этого срока можно говорить лишь о вероятности того или иного исхода беременности.
Кроме того, что аномальное прикрепление плаценты часто связано с ее неправильным контуром и предлежанием, существуют исследования, показывающие взаимосвязь глубокого прикрепления плаценты с аномалиями развития матки. Так, рlacenta accreta в рудиментарном роге матки впервые описана P.K. Heinonen в 1983 году [4]. M. Basbug et al. (1997) проанализировал 51 случай течения беременностей в рудиментарном роге матки, в 7 (13,7%) случаях отмечено наличие placenta accreta, т.е. беременность в рудиментарном роге значительно чаще ассоциируется с ней, чем обычная маточная беременность [1]. Сегодня все еще существуют большие проблемы в клинической диагностике этой патологии, в 40-60% случаев роды заканчиваются гистероэктомией не только по поводу кровотечения, но и из-за отсутствия своевременной диагностики.
Большую помощь в выявлении placenta accreta/increta/ percreta в динамике беременности оказывает цветное допплеровское картирование (ЦДК). Чувствительность и специфичность этого метода для диагностики placenta increta очень высока, особенно расположенной по передней стенке матки, т.е. патологическая маточно-пузырная гиперваскуляризация, вызванная ангиогенезом плацентарной инвазии, определяется с достаточно высокой степенью достоверности.
Выделяют следующие ультразвуковые признаки аномального прикрепления плаценты.
1. Диффузный или локальный интраплацентарно-лакунарный кровоток с высокоскоростным турбулентным потоком венозного типа.
2. Патологическое сосудистое соединение плаценты с мочевым пузырем с низкорезистентным артериальным плацентарным кровотоком (рис.3).
3. Расширение периферических субплацентарных васкулярных каналов с венозным пульсационным потоком над шейкой матки.
Именно эти признаки позволили нам своевременно предположить наличие плотного прикрепления плаценты на фоне предлежания в обоих рассматриваемых выше случаях.
При расположении плаценты по боковым стенкам, также как и по задней стенке, визуализировать патологию при УЗИ значительно тяжелее. В этих случаях некоторые авторы рекомендуют использовать магнитно-резонансную томографию.
Описаны случаи ложноположительных результатов, вызванных варикозным расширением вен и неоваскуляризацией после предшествующего кесарева сечения. У таких пациенток необходимо точно идентифицировать патологические сосуды, связывающие плаценту с мочевым пузырем, а также локальный лакунарный поток вокруг подозрительного плацентарно-миометрального участка.
Единственным методом родоразрешения при центральном предлежании плаценты является кесарево сечение. С позиций доказательной медицины никаких данных на основании контролируемых клинических исследований в поддержку других способов ведения беременных женщин с предлежанием плаценты не опубликовано. Однако оптимальное время для родов у таких пациенток продолжает дискутироваться, несмотря на то, что целесообразность выжидательного наблюдения до 37 недели признают практически все специалисты. Некоторые клиницисты, опасаясь кровотечения в поздние сроки беременности, рекомендуют плановое родоразрешение после 34-й недели беременности с предварительным исследованием амниотической жидкости на уровень зрелости легких у плода.
Активное ведение рожениц с предлежанием плаценты должно включать обеспечение безопасности оперативного вмешательства (квалификация врачей операционной бригады, наличие аппаратуры слежения, проведение мероприятий интенсивной терапии в ранний послеоперационный период).
Учитывая вероятность развития кровотечения, сложность прогнозирования этого осложнения в ходе операции, возникает проблема безопасного возмещения кровопотери, которое с экономическим эффектом обеспечивает такая процедура, как аутодонорство.
В настоящее время во всем мире наблюдается тенденция к ограничению использования донорской крови в связи с опасностью инфицирования вирусами иммунодефицита человека, гепатитов В, С, D, цитомегалии, вирусом Эпштейна-Барр, губчатого энцефалита крупного рогатого скота и другими; бактериями (бледная трепонема), простейшими (возбудители малярии). Кроме того, многие исследователи убедительно доказали, что переливание даже тщательно совмещенной донорской крови сопровождается иммунологическими реакциями, что может привести к депрессии иммунной системы, пирогенным и аллергическим реакциям.
Достоинствами аутодонорства, как лечебного мероприятия, когда больной выступает одновременно в роли донора и реципиента крови или ее компонентов, являются отсутствие аллоиммунизации, исключение риска передачи инфекций, существенное уменьшение риска трансфузионных реакций и потребности в аллогенных компонентах крови, стимуляция эритропоэза, благодаря чему обеспечивается большая безопасность заместительной трансфузионной терапии компонентами крови. Отсутствие банков крови в Украине (хотя консервация и забор стволовых клеток становится более популярным, что, вероятно, продвинет и проблему аутодонорства), отсутствие пропаганды аутодонорства требуют отдельного подхода к проблеме восполнения кровопотери в каждом родовспомогательном учреждении и дальнейшего развития этого метода в стране.
В описанных нами случаях женщины находились под наблюдением в отделении патологии беременности с 34-35 недели. Тщательный мониторинг состояния плода и матери позволил произвести плановое кесарево сечение после 37 недель.
Выводы
Таким образом, при наличии предлежания плаценты необходимо помнить о возможности ее плотного (глубокого) прикрепления. Наиболее информативным методом диагностики предлежания плаценты с аномальным прикреплением является УЗИ с применением ЦПК.
Ранняя диагностика и прогнозирование осложнений, связанных с предлежанием и аномальным прикреплением плаценты, адекватная подготовка и обеспечение необходимых мер для их ликвидации, способствовали в обоих описанных случаях безопасному проведению оперативного вмешательства и течению послеродового периода.
Литература
1. Basbug M., Soyuer I., Aygen E. Placenta accreta associated with rupture of a rudimentary horn pregnancy // In J Gynecol Obstet.– 1997. – V. 57. – P. 199-201.
2. Becker R.H., Vonk R. , Mende B.C., Ragosch V., Entezami M. The relevance of placental location at 20-23 gestational weeks for prediction of placenta previa at delivery: evaluation of 8650 cases // Ultrasound Obstet Gynecol. – 2001. – V. 17. – № 6. – P. 496-501.
3. Chou M.M., Ho E.S.K., Lee Y.H. Prenatal diagnosis of placenta previa accreta by transabdominal color Doppler ultrasound // Ultrasound Obstet Gynecol. – 2000. – V. 15. – № 1. – P. 28-35.
4. Heinonen P.K. Clinical implicationof the unicornuate uterus with rudimentary horn // Int J Gynecol Obstet. – 1983. – V. 21. – P. 145-150.
5. Mustafa S.A., Brizot M.L., Carvalho M.H.B. Transvaginal ultrasonography in predicting placenta previa at delivery: a longitudinal study // Ultrasound Obstet Gynecol. – 2002. – V. 20. – № 4. – P. 356-359. <?xml:namespace prefix = o ns = “urn:schemas-microsoft-com:office:office”>